1. Molekul Unsur
Molekul unsur adalah molekul yang terbentuk dari satu jenis atom saja. Contohnya adalah oksigen. Berdasarkan jumlah atom pembentuknya, molekul unsur dapat dibedakan sebagai berikut:
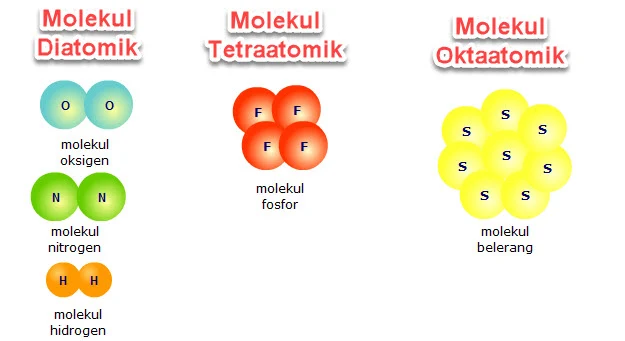
- Molekul Diatomik. Molekul Diatomik ini terbentuk dari dua atom yang sejenis. Contoh molekul diatomik adalah molekul oksigen, molekul hidrogen dan molekul nitrogen.
- Molekul Tetraatomik. Molekul tetraatomik ini terbentuk dari empat atom yang sejenis. Contoh molekul tetraatomik adalah molekul fosfor.
- Molekul Oktaatomik. Molekul oktaatomik ini terbentuk dari delapan atom yang sejenis. Contoh molekul tetraatomik adalah molekul sulfur (belerang).
| No. | Nama Unsur | Lambang Unsur | Rumus Molekul | Nama dan Jumlah Unsur Penyusun |
|---|---|---|---|---|
| 1. | Hidrogen | H | H₂ | Terdiri dari 2 atom hidrogen |
| 2. | Florida | F | F₂ | Terdiri dari 2 atom fluor |
| 3. | Oksigen | O | O₂ | Terdiri dari 2 atom oksigen |
| 4. | Nitrogen | N | N₂ | Terdiri dari 2 atom nitrogen |
| 5. | Klorida | Cl | Cl₂ | Terdiri dari 2 atom clor |
| 6. | Bromida | Br | Br₂ | Terdiri dari 2 atom brom |
| 7. | Iodida | I | I₂ | Terdiri dari 2 atom iodium |
| 8. | Phosfor | P | P₄ | Terdiri dari 4 atom fosfor |
| 9. | Sulfur | S | S₈ | Terdiri dari 8 atom sulfur |
| 10. | Astatin | At | At₂ | Terdiri dari 2 atom astatin |
2. Molekul Senyawa
Sebenarnya molekul senyawa banyak terdapat di kehidupan kita sehari-hari. Kita sering menggunakan atau terlibat dengan molekul senyawa tetapi kita jarang menyadarinya. Contohnya ketika kita minum atau mandi menggunakan molekul senyawa air (H₂O), ketika bernafas kita mengeluarkan molekul senyawa karbondioksida (CO₂), asap dari kendaraan bermotor sebagian mengandung senyawa molekul karbon monoksida (CO), dan cairan yang elektrolit aki adalah asam sulfat (H₂SO₄). Molekul senyawa adalah molekul yang terbentuk dari atom-atom yang berbeda.
Nah sekarang cobalah kalian perhatikan dengan cermat contoh molekul senyawa (molekul yang terdiri lebih dari satu jenis atom) berikut ini:
- Air (H₂O). Setiap molekul air terdiri dari dua atom hidrogen (H) dan satu atom oksigen (O).
- Karbon Monoksida (CO). Setiap molekul karbon monoksida terdiri dari satu atom karbon (C) dan satu atom oksigen (O).
- Karbon Dionoksida (CO2). Setiap molekul karbon dioksida terdiri dari satu atom karbon (C) dan dua atom oksigen (O).
- Kalium Hidroksida (KOH). Setiap molekul kalium hidroksida terdiri dari satu atom kalium (K), satu atom oksigen (O), dan satu atom hidrogen (H).
- Garam dapur (NaCl). Setiap molekul garam dapur terdiri dari satu atom natrium (Na), dan satu atom Klor (Cl).
Contoh Molekul Senyawa yang dapat dikonsumsi manusia langsung
| No. | Rumus Molekul | Nama dan Jumlah Unsur Penyusun | Nama Unsur |
|---|---|---|---|
| 1. | H₂O | Terdiri dari 2 atom hidrogen dan 1 atom oksigen | Air |
| 2. | C₆H₁₂O₆ | Terdiri dari 6 atom karbon, 12 atom hidrogen, dan 6 atom oksigen | Glukosa |
| 3. | C₁₂H₂₂O₁₁ | Terdiri dari 12 atom karbon, 22 atom hidrogen, dan 11 atom oksigen | Sukrosa |
| 4. | NaCl | Terdiri dari 1 atom natrium dan 1 atom klor | Garam Dapur |
| 5. | CH₃COOH | Terdiri dari 2 atom karbon, 4 atom hidrogen, dan 2 atom oksigen | Asam Cuka |
| 6. | NaHCO₃ | Terdiri dari 1 atom natrium, 1 atom hidrogen, 1 atom karbon, dan 3 atom oksigen | Soda Kue |
| 7. | CO(NH₂)₂ | Terdiri dari 1 atom karbon, 1 atom oksigen, 2 atom nitrogen, dan 4 atom hdirogen | Urea |
| 8. | C₂H₅OH | Terdiri dari 2 atom karbon, 5 atom nidrogen, 1 atom oksigen, dan 1 atom hidrogen | Ethanol |
| 9. | NH₃ | Terdiri dari 1 atom nitrogen, dan 3 atom hidrogen | Amonia |
| 10. | NaOH | Terdiri dari 1 atom natrium dan 1 atom oksigen, dan 1 atom hidrogen | Soda Api |
C. Campuran
Campuran merupakan materi yang terdiri dari dua atau lebih senyawa. Materi yang kita jumpai sehari-hari hampir semuanya campuran. Bahkan kita sering membuat campuran bahan, misalnya ketika kita membuat kopi atau teh manis. Campuran dibedakan menjadi tiga jenis, yaitu: Larutan, Koloid, dan Suspensi.
- Larutan adalah campuran yang homogen. Contoh larutan misalnya gula dan air. Gula (tidak terbedakan) lagi dari air . Campuran itu tampak homogen dan mempunyai komposisi yang sama pada setiap bagiannya. Zat dalam larutan tidak dapat dipisahkan melalui penyaringan.
- Suspensi adalah campuran kasar dan bersifat heterogen. Campuran ini awalnya tampak seperti larutan yang keruh, tetapi lambat laun terpisah karena pengaruh gravitasi (mengalami pengendapan). Suspensi dapat dipisahkan melalui penyaringan. Contoh suspensi yang lain misalnya kapur dengan air, tanah dengan air.
- Koloid adalah suatu bentuk campuran yang keadaannya antara suspensi dan larutan. Contoh koloid adalah air susu, santan, air sabun, dan cat. Koloid tampak keruh tetapi stabil (tidak memisah / mengendap). Bahan dalam campuran koloid tidak dapat dipisahkan melalui penyaringan.










0 komentar:
Post a Comment
Mohon tidak memasukan link aktif.